文章出處:法規(guī)動(dòng)態(tài) 網(wǎng)責(zé)任編輯: 金飛鷹 閱讀量: 發(fā)表時(shí)間:2024-11-15
近日,河北省藥監(jiān)局發(fā)布《關(guān)于進(jìn)一步做好行政許可告知承諾制工作的通知》(以下簡(jiǎn)稱(chēng)《通知》),其中提到,藥品、醫(yī)療器械互聯(lián)網(wǎng)信息服務(wù)審批、醫(yī)療單位使用放射性藥品(一、二類(lèi))許可、化妝品生產(chǎn)延續(xù)許可、藥品零售企業(yè)經(jīng)營(yíng)許可(僅從事乙類(lèi)非處方藥零售活動(dòng))等4項(xiàng)行政許可事項(xiàng)(詳見(jiàn)下方圖片)實(shí)行告知承諾制,相關(guān)監(jiān)管部門(mén)需加強(qiáng)審批和監(jiān)管工作。
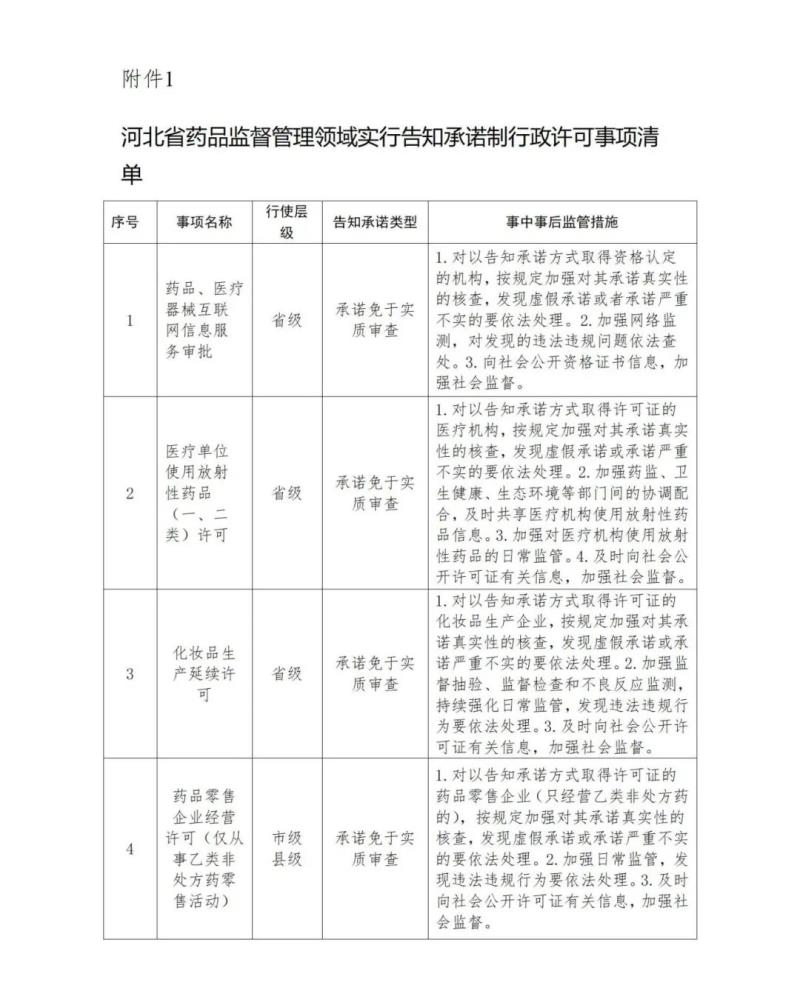
《通知》全文如下:
一、進(jìn)一步加強(qiáng)告知承諾制事項(xiàng)管理 各級(jí)行政審批部門(mén)和藥品監(jiān)管部門(mén)要持續(xù)依法依規(guī)做好已明確實(shí)行告知承諾制的藥品、醫(yī)療器械互聯(lián)網(wǎng)信息服務(wù)審批、醫(yī)療單位使用放射性藥品(一、二類(lèi))許可、化妝品生產(chǎn)延續(xù)許可、藥品零售企業(yè)經(jīng)營(yíng)許可(僅從事乙類(lèi)非處方藥零售活動(dòng))等4項(xiàng)行政許可事項(xiàng)(附件1)的審批和監(jiān)管工作。要嚴(yán)格按照《國(guó)務(wù)院辦公廳關(guān)于全面推行證明事項(xiàng)和涉企經(jīng)營(yíng)許可事項(xiàng)告知承諾制的指導(dǎo)意見(jiàn)》(國(guó)辦發(fā)〔2020〕42號(hào))關(guān)于法律、行政法規(guī)、國(guó)務(wù)院決定設(shè)定涉企行政許可事項(xiàng)實(shí)行告知承諾制的有關(guān)要求,依法依規(guī)確定實(shí)行告知承諾制行政許可事項(xiàng)范圍,持續(xù)強(qiáng)化告知承諾制行政許可事項(xiàng)管理不得隨意擴(kuò)大告知承諾制行政許可事項(xiàng)范圍。 二、進(jìn)一步規(guī)范告知承諾制工作運(yùn)行 (一)動(dòng)態(tài)完善實(shí)施標(biāo)準(zhǔn)。省局根據(jù)政策法規(guī)和國(guó)家局行政許可實(shí)施規(guī)范,動(dòng)態(tài)調(diào)整我全省藥監(jiān)系統(tǒng)行政許可實(shí)施規(guī)范,及時(shí)更新事項(xiàng)名稱(chēng)、設(shè)定依據(jù)、許可條件、申請(qǐng)材料等實(shí)施要素信息。各級(jí)行政審批部門(mén)要會(huì)同藥品監(jiān)管部門(mén)根據(jù)政策法規(guī)、行政許可實(shí)施規(guī)范調(diào)整情況,參照《河北省行政許可案卷標(biāo)準(zhǔn)(2024年版)》中行政許可告知承諾書(shū)文書(shū)樣式(附件2),結(jié)合工作實(shí)際,及時(shí)更新完善辦事指南和告知承諾書(shū)文本,并在省政務(wù)服務(wù)網(wǎng)公開(kāi),方便申請(qǐng)人查閱、下載和使用。 (二)持續(xù)規(guī)范審批流程。申請(qǐng)人按照行政審批部門(mén)告知的內(nèi)容,提交告知承諾書(shū)等申請(qǐng)材料。行政審批部門(mén)要按照省政府有關(guān)規(guī)定,嚴(yán)格審核受理?xiàng)l件,對(duì)符合適用條件的,應(yīng)當(dāng)按照告知承諾工作流程辦理。經(jīng)審查,申請(qǐng)人符合適用告知承諾的情形、承諾符合許可條件并按要求提交材料的,應(yīng)當(dāng)當(dāng)場(chǎng)作出行政許可決定,相關(guān)證照批文依法送達(dá)申請(qǐng)人,同時(shí)將許可信息同步推送至同級(jí)藥品監(jiān)管部門(mén),并依法向社會(huì)公開(kāi)許可信息。涉及現(xiàn)場(chǎng)勘驗(yàn)等特殊環(huán)節(jié)的,一律由審批前實(shí)施調(diào)整為審批決定后,統(tǒng)一由行業(yè)監(jiān)管部門(mén),通過(guò)事中事后監(jiān)管實(shí)施。 (三)扎實(shí)開(kāi)展履諾核查。各級(jí)藥品監(jiān)管部門(mén)要按照省政府有關(guān)規(guī)定,依法履行事中事后監(jiān)管責(zé)任,在行政審批部門(mén)作出準(zhǔn)予行政許可決定后60個(gè)工作日內(nèi),對(duì)申請(qǐng)人承諾內(nèi)容是否屬實(shí)進(jìn)行核查,依法履行事中事后監(jiān)管責(zé)任。對(duì)涉及社會(huì)公共利益、第三方利益平衡的事項(xiàng),原則上應(yīng)當(dāng)在7個(gè)工作日內(nèi)進(jìn)行核查。核查時(shí)限要求更短的或國(guó)家藥品監(jiān)督管理局對(duì)核查時(shí)限另有規(guī)定的,從其規(guī)定。各級(jí)藥品監(jiān)管部門(mén)應(yīng)當(dāng)在核查結(jié)束后5個(gè)工作日內(nèi)將核查信息推送至同級(jí)行政審批部門(mén)。 (四)依法追究違諾承責(zé)任。各級(jí)藥品監(jiān)管部門(mén)在核查或日常監(jiān)管中發(fā)現(xiàn)存在不實(shí)承諾或違反承諾情形的,責(zé)令其限期整改;逾期不整改或者整改后仍不符合條件的,應(yīng)當(dāng)依法依規(guī)予以查處,并及時(shí)告知行政審批部門(mén)依法撤銷(xiāo)行政許可決定;涉嫌犯罪的,依法移送司法機(jī)關(guān)。行政審批部門(mén)依法撤銷(xiāo)行政許可決定后,要及時(shí)告知相關(guān)同級(jí)藥品監(jiān)管部門(mén)。藥品監(jiān)管部門(mén)應(yīng)當(dāng)將申請(qǐng)人失信信息納入信用檔案,并將相關(guān)失信信息向省信用信息共享平臺(tái)歸集,作為分級(jí)分類(lèi)監(jiān)管依據(jù)。 三、進(jìn)一步強(qiáng)化事中事后監(jiān)管 (一)持續(xù)強(qiáng)化審管協(xié)同聯(lián)動(dòng)。各級(jí)行政審批部門(mén)和藥品監(jiān)管部門(mén)要持續(xù)強(qiáng)化部門(mén)協(xié)同,建立健全實(shí)施告知承諾制工作的協(xié)同對(duì)接和風(fēng)險(xiǎn)防范工作機(jī)制,及時(shí)共享有關(guān)數(shù)據(jù)信息,有效排查化解審管過(guò)程中的各類(lèi)風(fēng)險(xiǎn),確保行政審批與核查監(jiān)管工作的有效銜接,促進(jìn)服務(wù)質(zhì)量與監(jiān)管效能同步提升。 (二)不斷創(chuàng)新完善監(jiān)管方式。各級(jí)藥品監(jiān)管部門(mén)要按照“四個(gè)最嚴(yán)”要求,綜合運(yùn)用重點(diǎn)監(jiān)管、智慧監(jiān)管、協(xié)同監(jiān)管、信用監(jiān)管等監(jiān)管方式,通過(guò)檢查、檢驗(yàn)、監(jiān)測(cè)等手段,不斷完善監(jiān)管機(jī)制,強(qiáng)化事中事后監(jiān)管,加強(qiáng)投訴舉報(bào)的調(diào)查處理,依法查處虛假承諾、非法生產(chǎn)經(jīng)營(yíng)使用等違法違規(guī)行為,督促企業(yè)持續(xù)依法合規(guī),守牢藥品安全底線(xiàn)。 本通知自印發(fā)文之日起執(zhí)行,《河北省藥品監(jiān)督管理局關(guān)于落實(shí)深化行政許可告知承諾制改革的通知》(冀藥監(jiān)法函〔2022〕600號(hào))同時(shí)廢止。法律、法規(guī)、規(guī)章等另有規(guī)定的,從其規(guī)定。
行業(yè)藍(lán)皮書(shū)發(fā)布!我國(guó)醫(yī)療器械企業(yè)去年?duì)I收約12400億元
醫(yī)療器械注冊(cè)咨詢(xún)認(rèn)準(zhǔn)金飛鷹 深圳:0755-86194173 廣州:020 - 82177679 四川:028 - 68214295 湖南:0731-22881823 湖北:181-3873-5940 江蘇:135-5494-7827 廣西:188-2288-8311 海南:135-3810-3052 重慶:135-0283-7139