文章出處:企業(yè)原創(chuàng) 網(wǎng)責任編輯: 金飛鷹 閱讀量: 發(fā)表時間:2024-02-28
醫(yī)療器械臨床評價是采用科學合理的方法對臨床數(shù)據(jù)進行評價、分析,以確認醫(yī)療器械在其適用范圍下的安全性、臨床性能和/或有效性的持續(xù)進行的活動。這一過程中形成的資料也是醫(yī)療器械注冊申報中的一項核心資料。此前我們跟大家分享過不少有關(guān)臨床評價的內(nèi)容(戳右側(cè)查看合集→臨床評價),今天就再跟大家聊聊臨床數(shù)據(jù)的分析。
醫(yī)療器械臨床評價一般分為三個階段,第一階段是臨床評價的數(shù)據(jù)/文件來源(如文獻檢索、臨床經(jīng)驗或臨床試驗等),第二階段是臨床數(shù)據(jù)的評估,第三階段則是臨床數(shù)據(jù)的分析,那么到底應(yīng)如何對臨床數(shù)據(jù)進行分析呢?
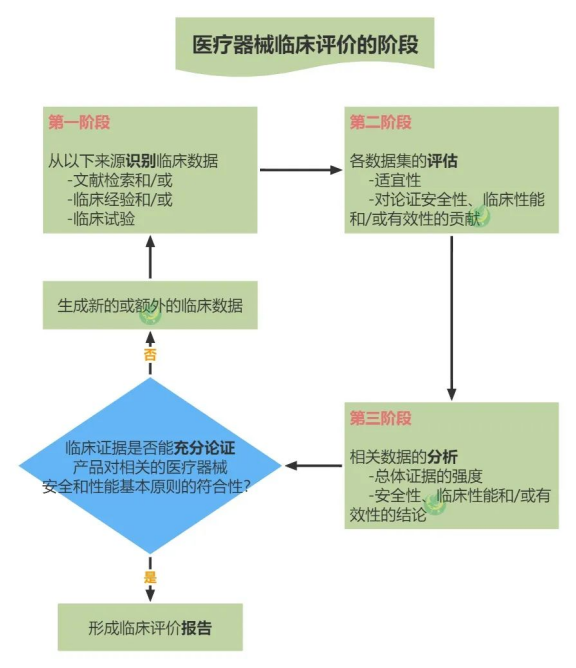
分析階段需確定,經(jīng)評估適用的臨床數(shù)據(jù)集,是否可用于產(chǎn)品的風險/受益分析,產(chǎn)品安全性、臨床性能和/或有效性的論證。
臨床數(shù)據(jù)的分析方法包括定量分析和定性分析。鑒于目前多數(shù)產(chǎn)品為漸進性設(shè)計變更,對臨床試驗的需求有限,其臨床評價將大量使用臨床文獻數(shù)據(jù)和臨床經(jīng)驗數(shù)據(jù),可能將使用定性分析方法(如描述性方法)。
使用評估階段制定的評價標準,對證明產(chǎn)品安全性、臨床性能和/或有效性的數(shù)據(jù)集進行評價。對數(shù)據(jù)集的結(jié)果進行研究,識別產(chǎn)品性能與風險在不同數(shù)據(jù)集之間的一致性。如不同數(shù)據(jù)集的結(jié)果相似,將增加產(chǎn)品安全性、臨床性能和/或有效性的確定性。如不同數(shù)據(jù)集的結(jié)果不一致,需明確造成差異的原因。不管結(jié)果如何,臨床評價需納入所有數(shù)據(jù)集。
最后,臨床評價人員需考慮,臨床證據(jù)與其他設(shè)計驗證和確認文件、器械描述、說明書和標簽、風險分析以及生產(chǎn)信息進行綜合分析時,能夠確證:
1)產(chǎn)品達到預(yù)期性能;
2)產(chǎn)品未對患者或者使用者產(chǎn)生不適當?shù)陌踩詥栴};
3)與患者受益相比,器械使用有關(guān)的風險可接受;
4)符合安全和性能基本原則;
5)是否需要開展上市后研究。
以下因素需予以考慮:使用產(chǎn)品的患者數(shù)量、患者隨訪的類型和適當性、不良事件的數(shù)量及嚴重性、對已識別的危害相關(guān)風險評估的充分性、診斷或治療病癥的嚴重性以及自然病程。還應(yīng)考慮是否有可替代的診斷或治療方式,以及當前的診療水平。
需對說明書和標簽等文件進行審核,以確保其與臨床數(shù)據(jù)一致,且已列明所有危害以及其他相關(guān)臨床信息。
醫(yī)療器械注冊咨詢認準金飛鷹
深圳:0755-86194173
廣州:020 - 82177679
湖南:0731-22881823
四川:028 - 68214295