文章出處:公告通知 網(wǎng)責(zé)任編輯: 金飛鷹 閱讀量: 發(fā)表時(shí)間:2024-03-04
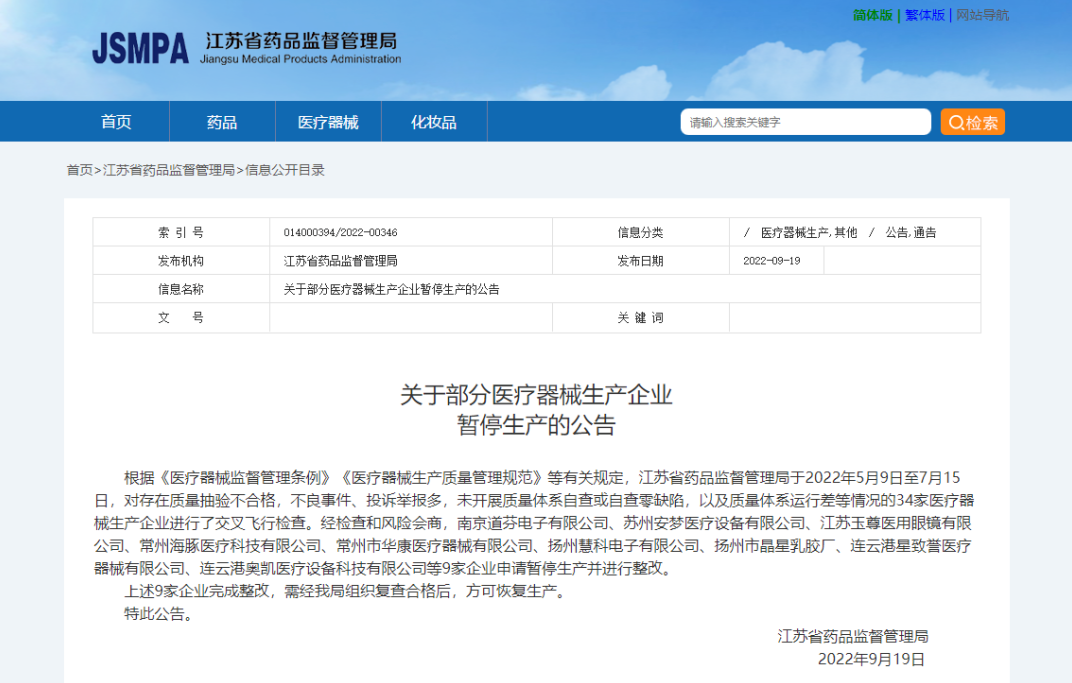
近日,江蘇省藥監(jiān)局官網(wǎng)發(fā)布關(guān)于部分醫(yī)療器械生產(chǎn)企業(yè)暫停生產(chǎn)的公告(以下簡(jiǎn)稱“公告”),公告指出,江蘇省藥品監(jiān)督管理局于2022年5月9日至7月15日,對(duì)存在質(zhì)量抽驗(yàn)不合格,不良事件、投訴舉報(bào)多,未開(kāi)展質(zhì)量體系自查或自查零缺陷,以及質(zhì)量體系運(yùn)行差等情況的34家醫(yī)療器械生產(chǎn)企業(yè)進(jìn)行了交叉飛行檢查。
經(jīng)檢查和風(fēng)險(xiǎn)會(huì)商,南京道芬電子有限公司、蘇州安夢(mèng)醫(yī)療設(shè)備有限公司、江蘇玉尊醫(yī)用眼鏡有限公司、常州海豚醫(yī)療科技有限公司、常州市華康醫(yī)療器械有限公司、揚(yáng)州慧科電子有限公司、揚(yáng)州市晶星乳膠廠、連云港星致譽(yù)醫(yī)療器械有限公司、連云港奧凱醫(yī)療設(shè)備科技有限公司9家企業(yè)申請(qǐng)暫停生產(chǎn)并進(jìn)行整改。
上述9家企業(yè)完成整改,需經(jīng)江蘇省藥品監(jiān)督管理局組織復(fù)查合格后,方可恢復(fù)生產(chǎn)。
醫(yī)療器械GMP的重要性
信息來(lái)源:江蘇省藥監(jiān)局
排版整理:金飛鷹藥械
醫(yī)療器械注冊(cè)咨詢認(rèn)準(zhǔn)金飛鷹
深圳:0755-86194173
廣州:020 - 82177679
湖南:0731-22881823
四川:028 - 68214295