根據《醫(yī)療器械注冊與備案管理辦法》第三十八條:
第三類醫(yī)療器械進行臨床試驗對人體具有較高風險的,應當經國家藥品監(jiān)督管理局批準。
臨床試驗審批是指國家藥品監(jiān)督管理局根據申請人的申請,對擬開展臨床試驗的醫(yī)療器械的風險程度、臨床試驗方案、臨床受益與風險對比分析報告等進行綜合分析,以決定是否同意開展臨床試驗的過程。
需進行臨床試驗審批的第三類醫(yī)療器械目錄由國家藥品監(jiān)督管理局制定、調整并公布。需進行臨床試驗審批的第三類醫(yī)療器械臨床試驗應在符合要求的三級甲等醫(yī)療機構開展。
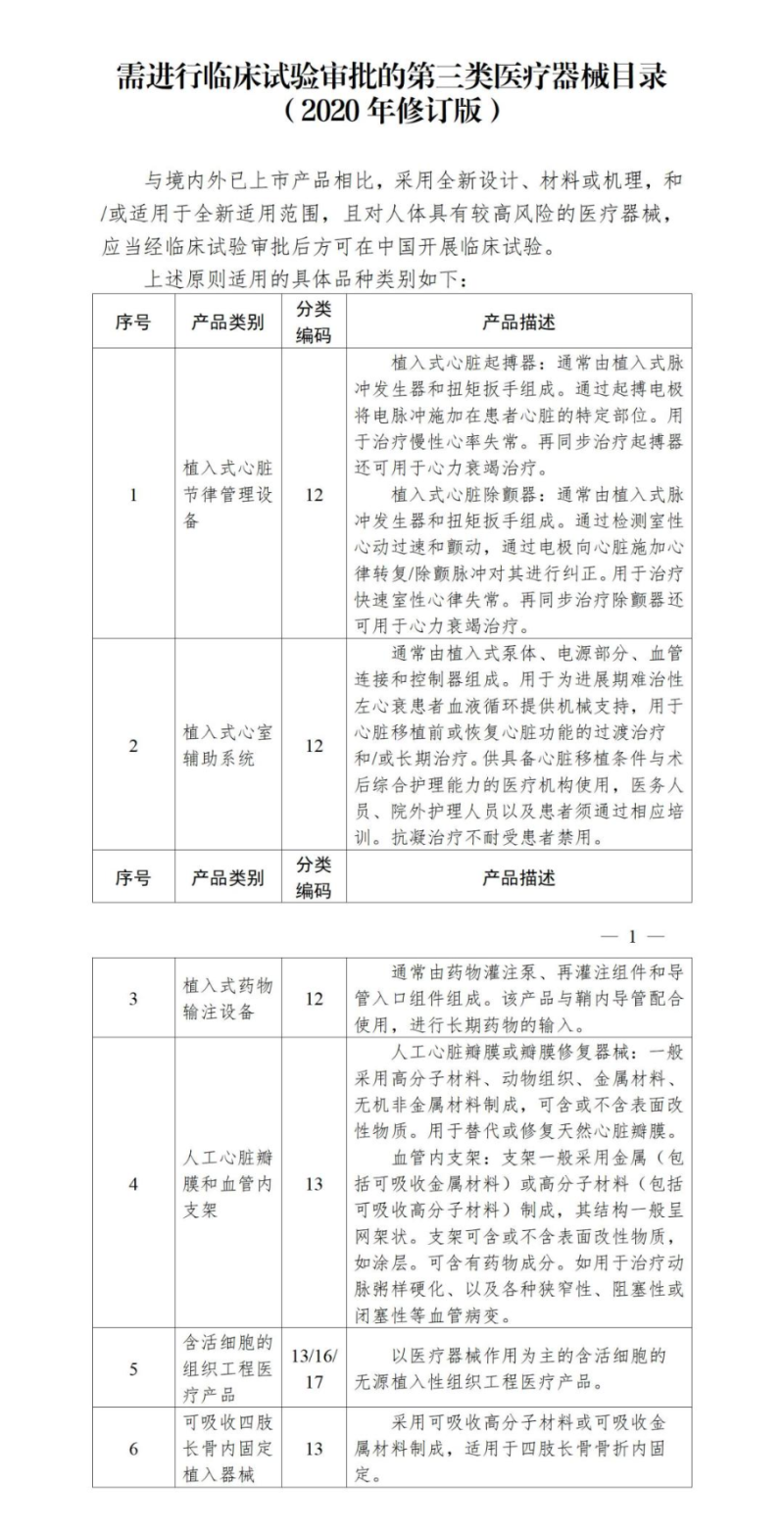
那么目前有哪些醫(yī)療器械產品需進行臨床試驗審批呢?根據《國家藥監(jiān)局關于發(fā)布需進行臨床試驗審批的第三類醫(yī)療器械目錄(2020年修訂版)的通告(2020年第61號)》,需進行臨床試驗審批的第三類醫(yī)療器械產品具體如下:
醫(yī)療器械注冊咨詢認準金飛鷹 深圳:0755-86194173 廣州:020 - 82177679 湖南:0731-22881823 四川:028 - 68214295