文章出處:行業(yè)干貨 網(wǎng)責任編輯: 金飛鷹 閱讀量: 發(fā)表時間:2024-02-29
隨著我國醫(yī)美行業(yè)的迅速發(fā)展,作為醫(yī)美入門項目之一的水光針,相信大家都再熟悉不過了。我們此前也跟大家科普過,水光針的主要成分為透明質(zhì)酸鈉,注射用透明質(zhì)酸鈉在我國是第三類醫(yī)療器械。事實上,假如要將透明質(zhì)酸鈉注射至真皮層,是需要有資質(zhì)的專業(yè)人員配合一系列配套器具使用的,這其中包括注射器、注射針以及助推裝置。
6月9日,金飛鷹輔導的深圳一家企業(yè)成功取得【皮下電子注射器控制助推裝置】的國內(nèi)Ⅱ類醫(yī)療器械注冊證,這是我們在醫(yī)美產(chǎn)品注冊輔導上的又一個重要里程碑。

本期文章我們就來簡單介紹一下此類產(chǎn)品國內(nèi)注冊的相關事項。
根據(jù)《2020年第一批醫(yī)療器械產(chǎn)品分類界定結(jié)果匯總》,“按照Ⅱ類醫(yī)療器械管理的產(chǎn)品(199個)”第13條:“皮下電子注射器控制助推裝置由主機、注射手具、腳踏開關、電源線、電源適配器及電子注射器控制軟件組成。需配合一次性使用無菌注射器及一次性使用無菌注射針使用。用于面部真皮層注射透明質(zhì)酸鈉。不與身體或注射的透明質(zhì)酸鈉接觸。可控制注入藥量、注射頻率等。分類編碼:14-01。”

需要特別指出的是,本次取證產(chǎn)品是專供醫(yī)療機構(gòu)使用的,我們在其注冊證的適用范圍也可以看到,“與注射器配合使用,供醫(yī)療機構(gòu)對患者面部真皮層進行定量注射透明質(zhì)酸鈉”。
電子注射器助推裝置注冊檢驗相關事項 如今我們在國家藥監(jiān)局官網(wǎng)搜索“助推裝置”,是可以搜索到部分產(chǎn)品的,但此類產(chǎn)品并不屬于《免于臨床評價醫(yī)療器械目錄》中的產(chǎn)品,因此,在產(chǎn)品注冊過程中,企業(yè)可查找已取得注冊證和醫(yī)療器械生產(chǎn)許可證且上市后無不良事件的同類產(chǎn)品,選擇這些同品種器械的臨床數(shù)據(jù)進行臨床評價。
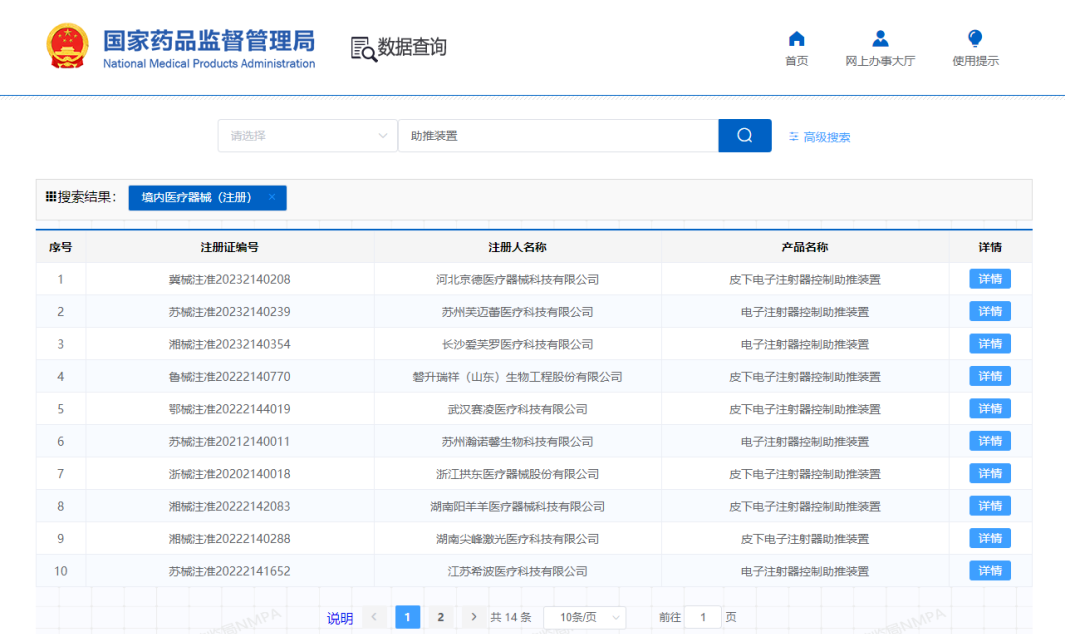
而在產(chǎn)品檢驗方面,首先,此類產(chǎn)品作為醫(yī)療器械里的有源產(chǎn)品,安規(guī)、EMC都是必不可少的。安規(guī)應符合GB 9706.1-2020《醫(yī)用電氣設備 第1部分:基本安全和基本性能的通用要求》這一通用要求,EMC則應符合YY 9706.102-2021《醫(yī)用電氣設備 第1-2部分:基本安全和基本性能的通用要求 并列標準:電磁兼容 要求和試驗》的要求。
與此同時,針對此類產(chǎn)品還有一項強制性專標:GB 9706.224-2021《醫(yī)用電氣設備 第2-24部分:輸液泵和輸液控制器的基本安全和基本性能專用要求》,產(chǎn)品基本安全和性能等必須滿足專標要求;除此之外,為更好地對產(chǎn)品進行風險控制,還要按照YY 9706.108-2021《醫(yī)用電氣設備 第1-8部分:基本安全和基本性能的通用要求 并列標準:通用要求,醫(yī)用電氣設備和醫(yī)用電氣系統(tǒng)中報警系統(tǒng)的測試和指南》標準要求,做好設備報警系統(tǒng)/信號的相關設計。
其他重點關注事項
因為此類產(chǎn)品需與其他產(chǎn)品配合使用,在產(chǎn)品設計初期就應重點關注聯(lián)合使用的適配性;而產(chǎn)品的注射效果也需要進行動物試驗研究并提供動物試驗研究資料(包括試驗目的、實驗動物信息、受試器械和對照信息、動物數(shù)量、評價指標和試驗結(jié)果、動物試驗設計要素的確定依據(jù)等),作為注冊申報資料的一部分。
醫(yī)療器械注冊咨詢認準金飛鷹 深圳:0755-86194173 廣州:020 - 82177679 湖南:0731-22881823 四川:028 - 68214295