文章出處:公告通知 網(wǎng)責(zé)任編輯: 金飛鷹 閱讀量: 發(fā)表時(shí)間:2024-02-28

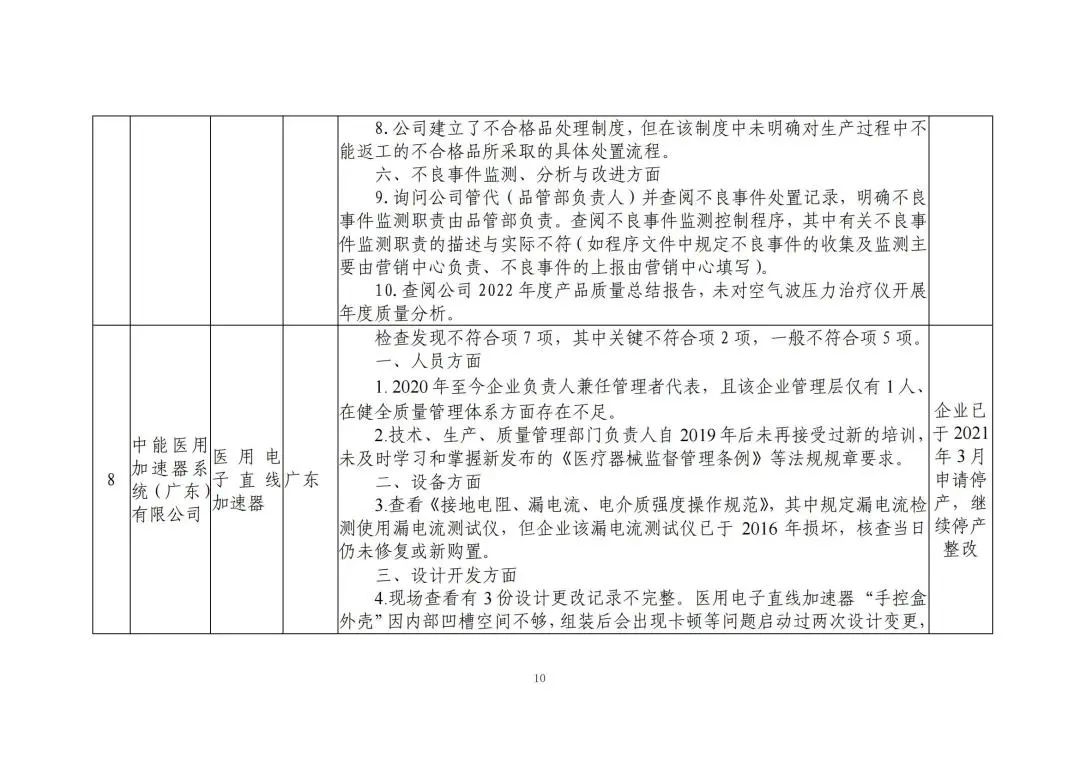
檢查發(fā)現(xiàn)不符合項(xiàng)7項(xiàng),其中關(guān)鍵不符合項(xiàng)2項(xiàng),一般不符合項(xiàng)5項(xiàng)。
01
人員方面
1. 2020 年至今企業(yè)負(fù)責(zé)人兼任管理者代表,且該企業(yè)管理層僅有1人、在健全質(zhì)量管理體系方面存在不足。
2. 技術(shù)、生產(chǎn)、質(zhì)量管理部門負(fù)責(zé)人自 2019 年后未再接受過新的培訓(xùn),未及時(shí)學(xué)習(xí)和掌握新發(fā)布的《醫(yī)療器械監(jiān)督管理?xiàng)l例》等法規(guī)規(guī)章要求。
02
設(shè)備方面
3. 查看《接地電阻、漏電流、電介質(zhì)強(qiáng)度操作規(guī)范》,其中規(guī)定漏電流檢測(cè)使用漏電流測(cè)試儀,但企業(yè)該漏電流測(cè)試儀已于2016年損壞,核查當(dāng)日仍未修復(fù)或新購置。
03
設(shè)計(jì)開發(fā)方面
4. 現(xiàn)場(chǎng)查看有3份設(shè)計(jì)更改記錄不完整。醫(yī)用電子直線加速器“手控盒外殼”因內(nèi)部凹槽空間不夠,組裝后會(huì)出現(xiàn)卡頓等問題啟動(dòng)過兩次設(shè)計(jì)變更,存在記錄填寫不完整(部分項(xiàng)目缺失、審批人未簽字),記錄中注明了經(jīng)裝配驗(yàn)證,但未能提供變更驗(yàn)證報(bào)告;醫(yī)用電子直線加速器“加速管防護(hù)鉛 B”因原切分設(shè)計(jì)不合理啟動(dòng)了設(shè)計(jì)變更,記錄中注明了經(jīng)裝配驗(yàn)證,但未能提供變更驗(yàn)證報(bào)告。企業(yè)執(zhí)行的 GB 15213-1994 標(biāo)準(zhǔn)更新為 GB 15213-2016,企業(yè)未針對(duì)設(shè)計(jì)變更的情況,對(duì)生產(chǎn)及檢驗(yàn)的規(guī)程做相應(yīng)修改。
04
采購方面
5. 查看關(guān)鍵物料“球管、平板”某供應(yīng)商評(píng)價(jià)記錄,該供方的醫(yī)療器械經(jīng)營(yíng)資質(zhì)證明文件已過期,但企業(yè)未重新對(duì)其相關(guān)資質(zhì)進(jìn)行收集和評(píng)價(jià)。
05
生產(chǎn)管理方面
6. 抽查企業(yè)兩個(gè)型號(hào)產(chǎn)品最后一個(gè)批次的生產(chǎn)記錄,記錄中缺少部分主要部件的序列號(hào)或者編號(hào),如旋轉(zhuǎn)機(jī)架、調(diào)制器、治療頭等。
06
質(zhì)量控制方面
7. 企業(yè)未按產(chǎn)品技術(shù)要求更新出廠檢驗(yàn)規(guī)程,現(xiàn)行檢驗(yàn)規(guī)程不能覆蓋產(chǎn)品技術(shù)要求的部分性能項(xiàng)目且缺少合理說明。抽查發(fā)現(xiàn)醫(yī)用電子直線加速器的出廠檢驗(yàn)規(guī)程和報(bào)告缺少產(chǎn)品技術(shù)要求中部分性能指標(biāo)。














信息來源:國(guó)家藥監(jiān)局食品藥品審核查驗(yàn)中心
排版整理:金飛鷹藥械
生產(chǎn)不符合經(jīng)注冊(cè)產(chǎn)品技術(shù)要求的醫(yī)療器械,湖南一公司被罰14.4萬
廣西藥監(jiān)局:2023年6月共批準(zhǔn)注冊(cè)強(qiáng)脈沖光治療儀等35個(gè)產(chǎn)品
湖南藥監(jiān)局:強(qiáng)脈沖光治療儀等35個(gè)醫(yī)療器械產(chǎn)品被終止注冊(cè)程序!
YY 0503-2023《環(huán)氧乙烷滅菌器》等20項(xiàng)醫(yī)械行業(yè)標(biāo)準(zhǔn)發(fā)布!
醫(yī)療器械注冊(cè)咨詢認(rèn)準(zhǔn)金飛鷹
深圳:0755-86194173
廣州:020 - 82177679
湖南:0731-22881823
四川:028 - 68214295