文章出處:行業(yè)干貨 網(wǎng)責(zé)任編輯: 金飛鷹 閱讀量: 發(fā)表時(shí)間:2024-03-07
2021年6月,新版《醫(yī)療器械監(jiān)督管理?xiàng)l例》(國(guó)務(wù)院第739號(hào)令)施行,其中明確規(guī)定“進(jìn)行醫(yī)療器械臨床評(píng)價(jià),可以根據(jù)產(chǎn)品設(shè)計(jì)特征、臨床風(fēng)險(xiǎn)、已有臨床數(shù)據(jù)等情形,通過(guò)開(kāi)展臨床試驗(yàn),或者通過(guò)對(duì)同品種醫(yī)療器械臨床文獻(xiàn)資料、臨床數(shù)據(jù)進(jìn)行分析評(píng)價(jià),證明醫(yī)療器械安全、有效”。
同品種臨床評(píng)價(jià)是臨床評(píng)價(jià)的一種路徑,是通過(guò)同品種產(chǎn)品的臨床數(shù)據(jù)完成申報(bào)產(chǎn)品的臨床評(píng)價(jià)。
1、同品種臨床評(píng)價(jià)是臨床評(píng)價(jià),還是臨床前研究的對(duì)比?
2、除了轉(zhuǎn)移生產(chǎn)、技術(shù)轉(zhuǎn)讓、基于上一代產(chǎn)品的改進(jìn),大多數(shù)情形下申報(bào)產(chǎn)品與同品種產(chǎn)品從原材料、生產(chǎn)過(guò)程到設(shè)計(jì)均存在不同程度的差異,如何認(rèn)為申報(bào)產(chǎn)品與同品種產(chǎn)品等同?
3、同品種產(chǎn)品已經(jīng)過(guò)上市前評(píng)價(jià)準(zhǔn)予上市,為何還要求申報(bào)產(chǎn)品的申請(qǐng)人收集同品種產(chǎn)品的臨床數(shù)據(jù)并進(jìn)行分析評(píng)價(jià)?
為了回答這些問(wèn)題,我們一起來(lái)看一下同品種評(píng)價(jià)的4個(gè)關(guān)鍵步驟:
1、同品種產(chǎn)品的選擇
2、申報(bào)產(chǎn)品與同品種產(chǎn)品進(jìn)行對(duì)比:若完全相同,按3、同品種產(chǎn)品臨床數(shù)據(jù)走;若存在差異,按4、差異性部分的安全有效性證據(jù)走。那么在步驟2,3,4中可能會(huì)存在以下問(wèn)題:我要對(duì)比什么項(xiàng)目?對(duì)比多少算充分?
3、同品種產(chǎn)品臨床數(shù)據(jù):提交的目的是什么?提交多少算充分?
4、差異性部分的安全有效性證據(jù):非臨床證據(jù)就夠了?還是一定要提交臨床證據(jù)?
(1)選擇目的:使用同品種產(chǎn)品的臨床數(shù)據(jù),開(kāi)展申報(bào)產(chǎn)品的臨床評(píng)價(jià)(借用數(shù)據(jù)、實(shí)現(xiàn)數(shù)據(jù)外推來(lái)完成申報(bào)產(chǎn)品的臨床評(píng)價(jià));
(2)如何選擇:與申報(bào)產(chǎn)品更為相似的產(chǎn)品(對(duì)申請(qǐng)者、監(jiān)管方都是最小負(fù)擔(dān));
(3)如何看待多個(gè)同品種產(chǎn)品:共同證明申報(bào)產(chǎn)品的安全有效性(證據(jù)集合)。
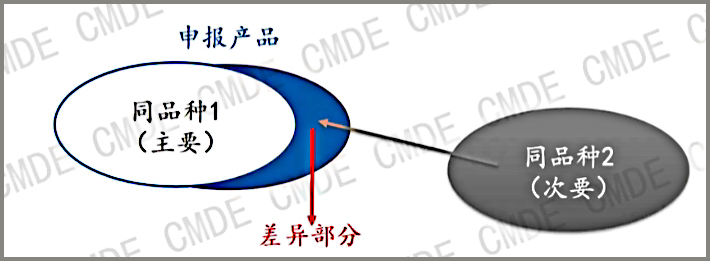
如圖所示,當(dāng)申報(bào)產(chǎn)品和同品種產(chǎn)品存在差異的時(shí)候,我們可能會(huì)引入第二個(gè)同品種產(chǎn)品即“同品種2”作為差異性的證據(jù),這個(gè)時(shí)候我們需要關(guān)注的是,不同的設(shè)計(jì)特征適用范圍在申報(bào)產(chǎn)品中組合時(shí)不應(yīng)相互影響。
參照法規(guī):醫(yī)療器械臨床評(píng)價(jià)技術(shù)指導(dǎo)原則(2021年第73號(hào))
一、技術(shù)特征
1.基本原理
2.結(jié)構(gòu)組成
3.生產(chǎn)工藝
4.制造材料
5.性能要求
6.軟件核心功能
7.安全性評(píng)價(jià)
8.符合的國(guó)家/行業(yè)標(biāo)準(zhǔn)
二、適用范圍及禁忌癥
9.適用范圍:(1)適用人群;(2)適用部位;(3)與人體接觸方式;(4)適應(yīng)癥
10.禁忌癥
三、產(chǎn)品說(shuō)明書(shū)臨床使用信息
11.使用方法
12.防范措施和警告
13.交付狀態(tài)、滅菌/消毒
14.包裝
15.標(biāo)簽
16.產(chǎn)品說(shuō)明書(shū)
開(kāi)展同品種臨床評(píng)價(jià)的,如使用了同品種產(chǎn)品非公開(kāi)數(shù)據(jù)(如生產(chǎn)工藝、臨床數(shù)據(jù)等),申請(qǐng)人應(yīng)提交使用授權(quán)書(shū),以保證數(shù)據(jù)來(lái)源的合法性;使用公開(kāi)發(fā)表的數(shù)據(jù),如公開(kāi)發(fā)表的文獻(xiàn)、數(shù)據(jù)、信息等,不需取得授權(quán)。
1、同品種臨床評(píng)價(jià)實(shí)質(zhì):使用同品種產(chǎn)品的臨床數(shù)據(jù)開(kāi)展申報(bào)產(chǎn)品的臨床評(píng)價(jià)(借用數(shù)據(jù)、實(shí)現(xiàn)數(shù)據(jù)外推來(lái)完成申報(bào)產(chǎn)品的臨床評(píng)價(jià));
2、數(shù)據(jù)來(lái)源:臨床試驗(yàn)數(shù)據(jù)、臨床經(jīng)驗(yàn)數(shù)據(jù)、臨床文獻(xiàn)數(shù)據(jù);
3、同品種臨床數(shù)據(jù)的作用:
a.確認(rèn)同品種產(chǎn)品的安全有效性在現(xiàn)有認(rèn)知下,是否已得到臨床公認(rèn),風(fēng)險(xiǎn)受益是否在可接受范圍內(nèi);
b.充分識(shí)別同品種產(chǎn)品的臨床有效性和使用風(fēng)險(xiǎn),為申報(bào)產(chǎn)品的風(fēng)險(xiǎn)受益分析提供信息;
c. 充分識(shí)別同品種產(chǎn)品的臨床風(fēng)險(xiǎn),為風(fēng)險(xiǎn)管理(最小化臨床風(fēng)險(xiǎn))提供信息;
d.基于同品種產(chǎn)品進(jìn)行設(shè)計(jì)變更的依據(jù);
e.為部分非臨床研究(如合架試驗(yàn))測(cè)試結(jié)果的評(píng)價(jià)提供臨床數(shù)據(jù)等。
當(dāng)申報(bào)產(chǎn)品與同品種產(chǎn)品存在差異時(shí),需提交充分的科學(xué)證據(jù)證明二者具有相同的安全有效性,從而論證其等同性。
1、增加具有可比性的同品種產(chǎn)品,提供臨床證據(jù);
2、非臨床研究(性能研究、臺(tái)架試驗(yàn)、動(dòng)物試驗(yàn));
3、申報(bào)產(chǎn)品的臨床證據(jù)。
醫(yī)療器械注冊(cè)咨詢認(rèn)準(zhǔn)金飛鷹 深圳:0755-86194173 廣州:020 - 82177679 湖南:0731-22881823 四川:028 - 68214295