一類體外診斷試劑進口備案變更
- 立即咨詢
-
全國服務熱線:
400-888-7587

400-888-7587
? 辦理條件 / Conditions
辦理備案的進口醫(yī)療器械體外診斷試劑,應當在備案人注冊地或者生產(chǎn)地址所在國家(地區(qū))獲得醫(yī)療器械醫(yī)療器械上市許可。境外備案人辦理進口醫(yī)療器械醫(yī)療器械備案,應當通過其在
中國境內(nèi)設立的代表機構或者指定中國境內(nèi)的企業(yè)法人作為代理人辦理。
政府官方原文鏈接:
http://www.nmpa.gov.cn/WS04/CL2138/299974.html
? 申請材料清單 / List of application materials
1、變化情況說明及相關證明文件 (1)變化情況說明應附備案信息表變化內(nèi)容比對列表。 (2)涉及產(chǎn)品技術要求變化的,應提供產(chǎn)品技術要求變化內(nèi)容比對表。 (3)變更產(chǎn)品名稱(體外診斷試劑為產(chǎn)品分類名稱,以下同)、產(chǎn)品描述、預期用途的,變更后的內(nèi)容應與第一類醫(yī)療器械產(chǎn)品目錄和相應體外診斷試劑子目錄相應內(nèi)容一致。其中,產(chǎn)品名稱應當與目錄所列內(nèi)容相同;產(chǎn)品描述、預期用途,應當與目錄所列內(nèi)容相同或者少于目錄內(nèi)容。 (4)相應證明文件應詳實、全面、準確。 2、證明性文件 境內(nèi)備案人提供:企業(yè)營業(yè)執(zhí)照副本復印件、組織機構代碼證副本復印件。 境外備案人提供: (1)如變更事項在境外備案人注冊地或生產(chǎn)地址所在國家(地區(qū))應當獲得新的醫(yī)療器械主管部門出具的允許產(chǎn)品上市銷售證明文件的,應提交新的上市證明文件。如該證明文件為復印件,應經(jīng)當?shù)毓C機關公證。 (2)境外備案人在中國境內(nèi)指定代理人的委托書、代理人承諾書及營業(yè)執(zhí)照副本復印件或者機構登記證明復印件。 | 3、符合性聲明 (1) 聲明符合醫(yī)療器械備案相關要求; (2)聲明本產(chǎn)品符合第一類醫(yī)療器械產(chǎn)品目錄和相應體外診斷試劑分類子目錄的有關內(nèi)容; (3) 聲明本產(chǎn)品符合現(xiàn)行國家標準、行業(yè)標準并提供符合標準的清單; (4) 聲明所提交備案資料的真實性。 |
? 辦理流程 / Processing process
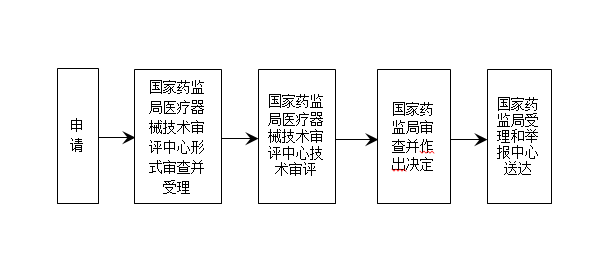
? 廣東政務局服務承諾時間 / Service Commitment Time of Guangdong Government Bureau
名稱 | 其他 | 時限 |
(工作日) | ||
(工作日) |
? 辦理依據(jù) / Processing basis
1. 法律法規(guī)名稱:《醫(yī)療器械監(jiān)督管理條例》 依據(jù)文號:國家食品藥品監(jiān)督管理總局關于第一類醫(yī)療器械備案有關事項的公告(第26號) |
? 金飛鷹相關服務 / Golden Eagle related services
●產(chǎn)品技術要求編制 ●產(chǎn)品說明書,標簽合規(guī)性審核 ●與產(chǎn)品有關的有關資料翻譯 ●產(chǎn)品送檢資料準備 ●公證文件格式提供及公證內(nèi)容審核 ●備案資料編制及遞交 |
? 結果樣本 / Results the sample
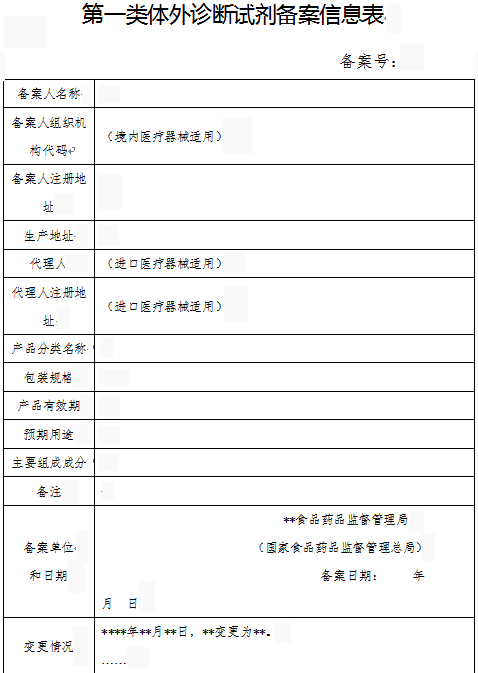
全面解決您的研發(fā)、生產(chǎn)、驗收、營銷全流程問題

practical experience
2000多個二、三類醫(yī)械項目經(jīng)驗沉淀,為你分配做過相同案例的實戰(zhàn)老師。
Professional translation
匯聚7大語種專業(yè)翻譯精英,多年醫(yī)械行業(yè)翻譯經(jīng)驗,能準確翻譯專業(yè)名詞及用語。
Software development
強大的軟件研發(fā)團隊,已為集團研發(fā)出成熟的項目管理軟件,可提供軟件定制服務。
Group supply chain
嚴選數(shù)十個優(yōu)秀的醫(yī)械行業(yè)服務機構,可為客戶推薦更實惠的醫(yī)械配套服務。
多次創(chuàng)造二三類高風險產(chǎn)品一次性通過的行業(yè)紀錄
項目狀態(tài):已結案
項目輔導老師:李老師
項目狀態(tài):已結案
項目輔導老師:車老師
項目狀態(tài):已結案
項目輔導老師:王老師
項目狀態(tài):已結案
項目輔導老師:黃老師